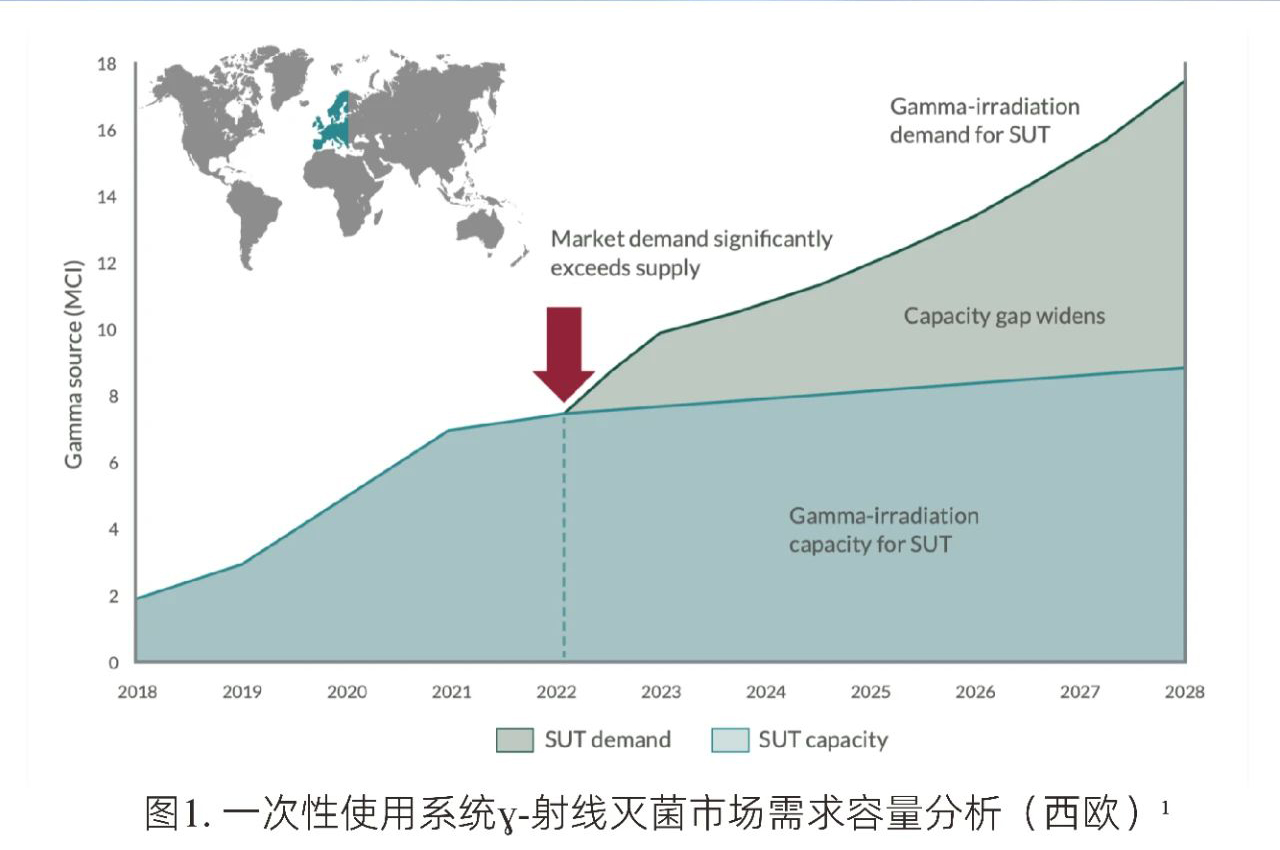
应用在医药行业的一次性使用技术(SUT)主要采用y-射线辐照(GI)进行灭菌,随着市场规模的增长,以及y-射线辐照源钴-60产量增长有限,截止2022年,西欧已经出现了Y-射线灭菌容量与SUT灭菌需求持平的现象。供需不平衡问题逐渐凸显,造成了y-灭菌市场供给不足及价格增长,亟需新的灭菌技术填充逐渐扩大的需求空白。
2021年,Bio-Process Systems Alliance(BPSA)发布了《一次性使用生物工艺设备的X-射线灭菌第一部分-行业需求、要求和风险评估》(X-RAY STERILIZATION OF SINGLE-USE BIOPROCESS EQUIPMENT PART I - INDUSTRY NEED, REQUIREMENTS AND RISK EVALUATION)²技术指南指出,X-射线(XI)可以作为有效且与GI灭菌等效替代的候选技术之一。2023年,BPSA又发布了《一次性使用生物工艺设备的X-射线灭菌第二部分-有代表性的确认数据》(PART II-REPRESENTATIVE QUALIFICATION DATA)3,总结了不同一次性组件GI和XI后的物理性能及功能性能可比性方面的代表性数据,以便于科学评价并支持相关变更工作和风险评估。


在以上两个BPSA指南的基础上,基于BioPhorum平台(著名的BPOG的所属生物药工业联盟组织),科百特与其他十家行业内著名国际药企(AZ,BMS,Eli Lily,GSK,Pfizer,Sanofi等)和供应商共同起草了《一次性使用系统X-射线辐照灭菌风险评估指南》(X-RAY STERILIZATION RISK ASSESSMENT - Guidance for risk evalua-tion of X-ray irradiation of single-use systems),旨在指导不同一次性使用系统开展GI到XI变更过程中风险评估如何具体开展,以及建议的变更风险级别如何定义的问题;该指南建立在国际药企之间的共识以及与FDA、EMA和日本相关药监组织充分沟通的基础上,具有相当的权威性,并提供了一个可操作的各种一次性组件的XI影响水平的风险评估工具包,方便药企开展变更评估工作。

指南的发布,为中国制药企业迎接不远的将来可能面临的一次性使用系统GI到XI灭菌方式的变更提供了经验。通过提供先验知识和建立可比性,减少GI到XI变更所需的相关风险评估,便于药企在收到供应商变更通知的第一时间,甚至可以提前有条不紊地主动开展变更风险评估工作。